Сказать "Спасибо"

Объяснение периодических свойств химических элементов (таблица Менделеева) на основе схемы Рассела-Саундерса.
Схема Рассела-Саундерса - схема построения волновых функций атомных состояний, основанная на представлении, что орбитальные моменты атомных электронов складывается в орбитальный момент атома  , а их спиновые моменты - в спин атома
, а их спиновые моменты - в спин атома 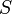 , которые взаимодействуют между собой.
Понимание периодической системы элементов основано на идее об оболоченной структуре электронного облака.
, которые взаимодействуют между собой.
Понимание периодической системы элементов основано на идее об оболоченной структуре электронного облака.
Каждый следующий атом получается из предыдущего добавлением заряда ядра на единицу 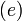 и добавлением одного электрона, который помещают в разрешенное принципом Паули состояние с наименьшей энергией.
и добавлением одного электрона, который помещают в разрешенное принципом Паули состояние с наименьшей энергией.
- Распределение электронов по состояниям называют электронной конфигурацией. Их обозначают символически, например, так:
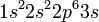
- Оболочку (или подоболочку), полностью заполненную электронами, называют замкнутой. Все три квантовых числа (
 ) у замкнутых оболочек (и подоболочек) равны нулю. Электроны в каждой подоболочке называют эквивалентными, у них одинаковы значения
) у замкнутых оболочек (и подоболочек) равны нулю. Электроны в каждой подоболочке называют эквивалентными, у них одинаковы значения  и
и 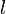 .
.
- Вплоть до атома
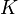 последовательность заполнения оболочек и подоболочек имеет "идеальный" характер. Первый "сбой" происходит с атомом
последовательность заполнения оболочек и подоболочек имеет "идеальный" характер. Первый "сбой" происходит с атомом 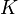 : внешний электрон занимает, вместо
: внешний электрон занимает, вместо 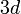 -состояния,
-состояния, 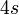 . Подобное - не единственный случай в периодической системе, и связано это с тем, что такие конфигурации оказываются более выгодными.
. Подобное - не единственный случай в периодической системе, и связано это с тем, что такие конфигурации оказываются более выгодными.