Сказать "Спасибо"
Вычисление свободной энергии и основных термодинамических величин больцмановского газа
Идеальный газ - газ, взаимодействие между частицами которого настолько слабо, что им можно пренебречь.
Применив к молекулам газа формулу распределения Гиббса, можем утверждать, что вероятность молекуле находиться в  -м состоянии, а потому и среднее число
-м состоянии, а потому и среднее число  молекул в этом состоянии, пропорциональны
молекул в этом состоянии, пропорциональны  :
:
 ,
,где  - постоянная определяемая условием нормировки:
- постоянная определяемая условием нормировки:
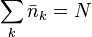
Распределение идеального газа, по различным состояниям, определяемое формулой (37.2) называется распределением Больцмана.
Применим формулу (31.3)

для вычисления свободной энергии идеального газа, подчиняющегося статистике Больцмана.
Подставляя это выражение в (41.1), получаем

Поскольку 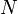 - очень большое число, то для
- очень большое число, то для  можно воспользоваться формулой (40.3). В результате получим следующую формулу
можно воспользоваться формулой (40.3). В результате получим следующую формулу
![F=-NT\ln\left[\frac{e}{N}\sum_ke^{-\varepsilon_k/T} \right]](8_teorphys/39/10.png)
Термодинамический потенциал
 .
.Энтропия определяется как

Энергия равна
 .
.