Сказать "Спасибо"
Зависимость теплоемкости газов от температуры.
В частности, для газа, состоящего из двухатомных молекул, теплоемкость складывается из поступательной, вращательной и колебательной частей и равна
 .
.Это значит, что теплоемкость должна быть постоянной. Вместе с тем опыт говорит, что теплоемкость зависит от температуры.
При понижении температуры "замораживаются" сначала колебательные степени свободы, а затем и вращательные степени свободы.
Согласно законам квантовой механики энергия гармонического осциллятора с классической частотой  может принимать только дискретный набор значений
может принимать только дискретный набор значений

В соответствии с распределением Гиббса вероятность того, что молекула обладает энергией 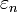 , равна
, равна

Найдем статистическую сумму

Зная величину  можно найти среднюю энергию молекулы:
можно найти среднюю энергию молекулы:

Для молярной теплоемкости получаем

получаем, что теплоемкость убывает до нуля. Причина - это дискретность уровней гармонического осциллятора.